-臨床成績〈成人〉-
臨床成績 -国内第Ⅲ相単盲検比較試験〈成人〉- 1,2)
1)フルティフォーム®国内第Ⅲ相長期投与試験〈成人〉(承認時評価資料).
2)東田有智 他. アレルギー・免疫. 2013; 20: 1686-704.
利益相反:本試験は杏林製薬株式会社の支援を受けて行われた
| 目的 |
フルティフォーム®の52週間長期投与による安全性及び有効性を検討する。 |
|---|---|
| 対象 |
16歳以上の気管支喘息患者244例(完了被験者214例) |
| 方法 |
非盲検非対照試験。2週間の観察期間の後、観察期で使用した吸入ステロイド薬(ICS)の用量に基づき、低用量群、中用量群、高用量群に割付け、52週間投与した。また、治療期間中、増量又は減量基準に合致した場合には、治験薬の増量又は減量を可能とした。 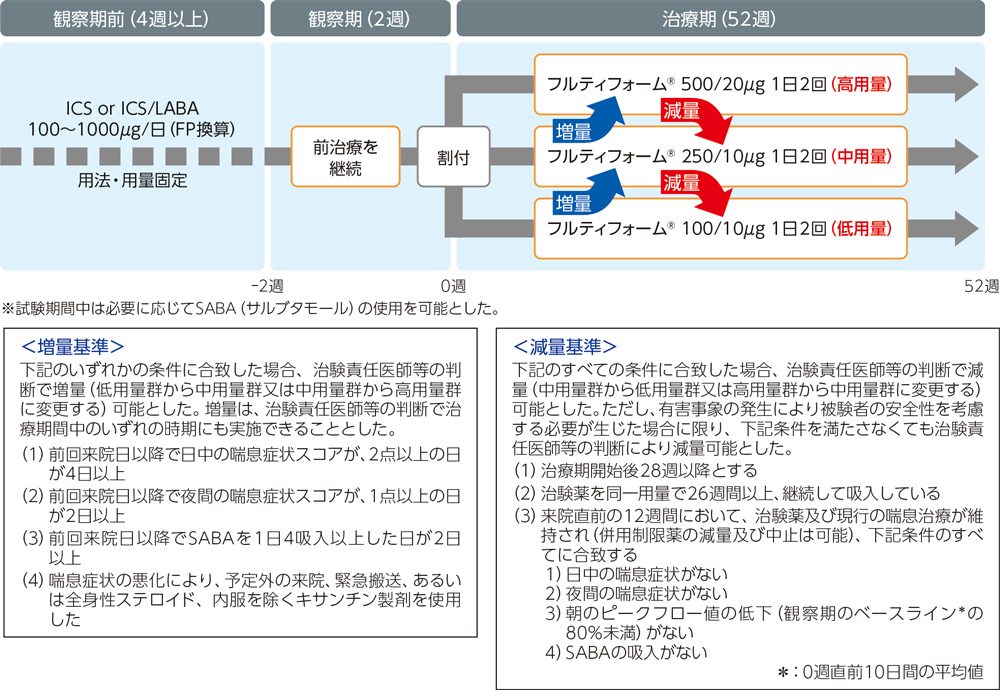
|
| 評価項目 |
|
| 解析計画 |
|
4. 効能又は効果
気管支喘息
(吸入ステロイド剤及び長時間作動型吸入β2刺激剤の併用が必要な場合)
6. 用法及び用量(抜粋)
成人
通常、成人には、フルティフォーム50エアゾール(フルチカゾンプロピオン酸エステルとして50μg及びホルモテロールフマル酸塩水和物として5μg)を1回2吸入、1日2回投与する。
なお、症状に応じてフルティフォーム125エアゾール(フルチカゾンプロピオン酸エステルとして125μg及びホルモテロールフマル酸塩水和物として5μg)を1回2~4吸入、1日2回投与する。
安全性(主要評価項目)
有害事象及び副作用
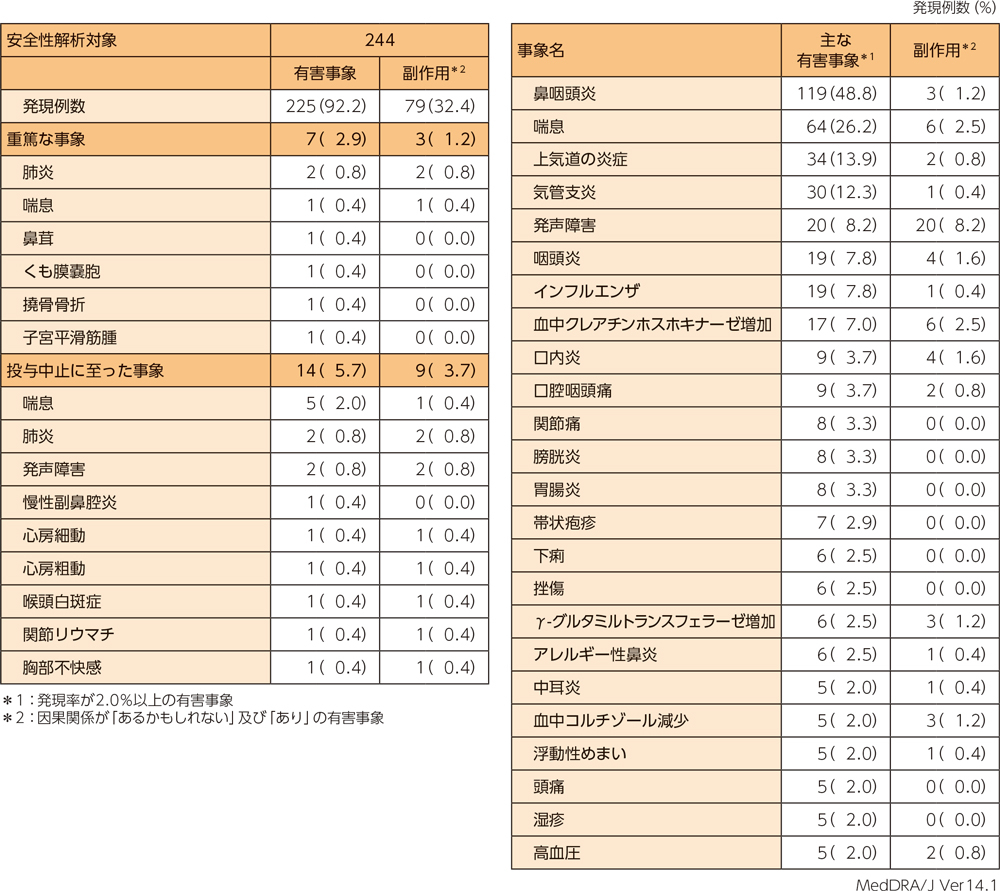
有害事象は244例中225例(92.2%)、副作用は244例中79例(32.4%)に認められた。重篤な有害事象、投与中止に至った有害事象、主な有害事象、主な副作用はそれぞれ以下のとおりであった。本試験において、死亡例は認められなかった。
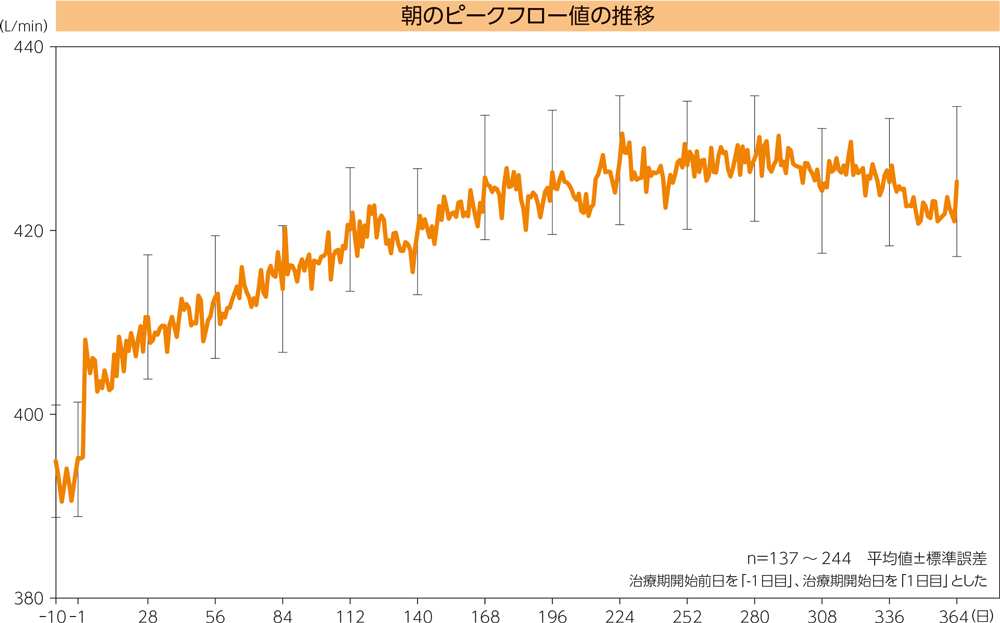
有効性(副次評価項目)〈朝のピークフロー値の推移〉2)
朝のピークフロー値はフルティフォーム®の投与後から52週にかけて下記のとおり推移した。
臨床成績 -海外第Ⅲ相比較試験〈成人〉:海外データ-
フルティフォーム®海外第Ⅲ相比較試験〈成人〉(承認時評価資料).
Bodzenta-Lukaszyk A et al. BMC Pulmonary Medicine. 2011; 11: 28. 一部改変
利益相反:本試験はMundipharma社の資金提供を受けて実施された
| 目的 |
フルティフォーム®(フルチカゾン/ホルモテロール配合剤)のフルチカゾン/サルメテロール配合剤に対する非劣性を検討し、更に気管支拡張作用発現の速さを比較検討する。 |
|---|---|
| 対象 |
18歳以上の軽症から重症持続型の気管支喘息患者202例 |
| 方法 |
非盲検無作為化実薬対照並行群間比較試験。4~10日間のスクリーニング期間の後、フルティフォーム®(100/10μgまたは250/10μgを1日2回)またはフルチカゾン/サルメテロール(100/50μgまたは250/50μgを1日2回)のいずれかを12週間投与した。 |
| 評価項目 |
|
| 解析計画 |
主要評価項目の最小二乗平均について、群間差の95 %信頼区間の下限が‒0.2L以上の場合、フルチカゾン/サルメテロールの非劣性が検証されたとした。p値は投与群と投与量を固定効果、ベースラインの投与前FEV1を共変量、実施医療機関を変量効果とするANCOVAを用いた。気管支拡張効果の作用発現までの時間については、多変量生存時間分析を用いた。 |
有効性評価項目
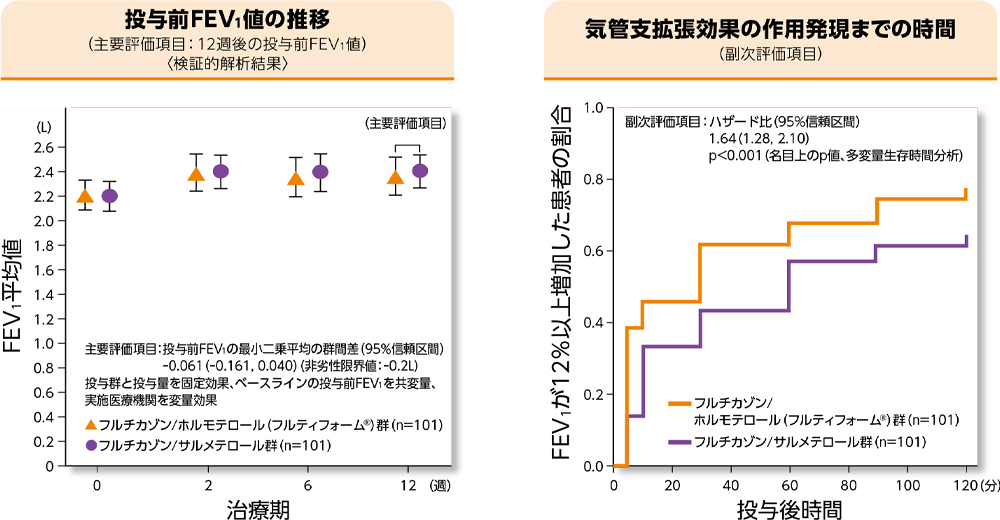
12週後の投与前FEV1について、最小二乗平均の群間差(95%信頼区間)は−0.061(−0.161, 0.040)であり、95%信頼区間の下限値が事前規定した非劣性の限界値(−0.2L)を上回ったため、フルチカゾン/サルメテロールに対するフルティフォーム®の非劣性が検証された。副次評価項目はハザード比(95%信頼区間)が1.64(1.28, 2.10)であり、気管支拡張効果の作用発現までの時間に有意差(p<0.001、名目上のp値、多変量生存時間分析)が認められた。
安全性評価項目
副作用はフルティフォーム®群で動悸が1例(1.0%)、フルチカゾン/サルメテロール群で呼吸困難が1例(1.0%)であった。

禁忌を含む注意事項等情報につきましては電子添文をご参照ください。

