藤城
がん遺伝子検査とがんゲノム医療についてお話をうかがいたいと思います。鹿毛先生は現在、呼吸器内科の教授ですが、その前はゲノム診療部で準教授をお務めでした。まず、がんゲノム医療体制につきまして、教えていただけないでしょうか。
鹿毛
初めに、がんゲノム医療が何をやっているかについてお話をします。もともと抗がん剤は、細胞増殖が盛んな細胞を殺してくれるものです。自分の正常な細胞はそこまでダメージを受けないので、がんの薬物治療のメインでしたが、がんゲノム医療というのは抗がん剤ではなく、分子標的薬を使うために行っています。
がんというのは、遺伝子に変異が起きることによってできてくる病気だと現在は考えられていますので、メインとなる遺伝子変異を見つけて、それに対して薬があれば、それを投与していたというのが、がんゲノム医療のはしりになると思います。
藤城
かなり多くの施設ですでに体制は整っていると考えてよいのでしょうか。
鹿毛
そうですね。実際に1つの遺伝子だけ調べるのではなくて、現在では100以上の遺伝子を同時に調べるがん遺伝子パネル検査を行っていて、それが保険で認められたのが2019年なので、もう6年経っています。
これは厚生労働省が、がんゲノム医療病院というのを決めていて、中核拠点病院と拠点病院と連携病院で全国300施設以上あります。それなりの数ではありますが、全国どの病院でもできる検査ではないという制約はあります。
藤城
がんの治療といいますと、殺細胞性抗がん剤がずっと使われてきたかと思います。患者さんも副作用でかなり苦しんでいたと思いますが、こういうゲノム医療ががん診療に入ってくると、患者さんの副作用も軽減されるという理解でよいのでしょうか。
鹿毛
そうですね。殺細胞性抗がん剤自体も、制吐剤や白血球を増やすGCSFなどの様々な支持療法によって副作用は軽減されていますが、分子標的薬はQOLを保つという意味では、さらにそれよりも良い薬だと思います。
藤城
具体的に肺がんの診療におけるがん遺伝子検査、もしくはがん遺伝子パネル検査の位置づけについて教えていただけますか。
鹿毛
肺がんは2000年頃、25年ぐらい前にEGFR阻害薬が承認され、当初ゲフィチニブが有名だったと思いますが、それがずっと続いてきています。初めはEGFR遺伝子だけを調べる時代が長かったので、パネル検査ではなくて1遺伝子検査でした。
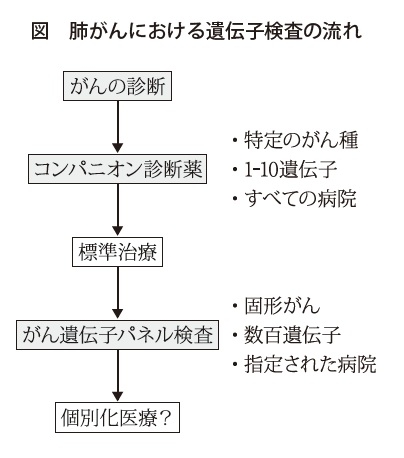
ただその後、ALK遺伝子やほかの様々な遺伝子が加わってきて、現在では9つを同時に調べられる小さなパネルをマルチプレックス遺伝子検査と呼んでいます。複数の遺伝子を同時に調べるものをコンパニオン診断薬といい、薬を投与するためには特定の検査で調べ、薬と検査をセットにしなければならないという制約があります。そのコンパニオン診断薬で幾つかの遺伝子を同時に調べ、それで該当するものがあれば薬を投与するという検査を、非小細胞肺がんについては診断時に行っています。
藤城
非小細胞肺がんという診断がついたときには9つの遺伝子を最初に調べ、そのうえでどういうレジメンで治療していくかが決まっていくという理解でよいですか。
鹿毛
はい。やはり遺伝子変異が見つかると、分子標的薬の効果は非常に高いです。奏効率といって、腫瘍が縮小する可能性は半分以上あって、腫瘍が大きくならないdisease control rateは8~9割です。抗がん剤を使ったり、免疫チェックポイント阻害薬も最近よく使っていますが、やはり効果は分子標的薬のほうが高いです。まずは遺伝子を調べて、該当する遺伝子変異があれば分子標的薬を投与し、もし何もなければ次の治療を考えるという順番になっています。
藤城
もしそのような検査で異常をきちんと検出することができて、適切な分子標的薬を投与した後、治療効果が十分得られなかった場合、もしくは一時効果を得られたけれども再増悪してくるような状況のときに、がん遺伝子パネル検査が登場してくるのでしょうか。
鹿毛
そうですね。そのような流れになります。がん遺伝子パネル検査というのは、標準治療が終わった患者さんか、終わる見込みがある進行性の固形がんの患者さんに対して保険適用となっていますので、診断時から行うことはできません。肺がんにおいては、まずは9種類の遺伝子を調べて、該当すれば分子標的薬になりますし、該当しなければほかの薬になって、後でがん遺伝子パネル検査を行うという順番で行っています。
藤城
がん遺伝子パネル検査を行って、実際に適切な分子標的薬、標的遺伝子が見つかる方は、肺がんの場合はどのぐらいいるのでしょうか。
鹿毛
非小細胞肺がんが肺がん全体の8割ぐらいで、その半分以上が腺がんになるので、肺がん全体でいうと、約半数が腺がんです。その約半分がこの分子標的薬の対象になるので、肺がんでいうと、全体の4分の1ぐらいに薬を届けられていると思います。
藤城
あとで行うのががん遺伝子パネル検査ということで、治療薬が見つかることは、それほど多くないのでしょうか。
鹿毛
はい。後日行うパネル検査では、それほど多くはないのですが、実は、コンパニオン診断薬を診断時に行って、何も遺伝子が見つからなかったので抗がん剤や免疫チェックポイント障害薬を使っていたような患者さんに後日がん遺伝子パネル検査を行うと、意外と当初なかったはずのEGFR遺伝子変異が見つかることがそれなりによくあることが我々の研究で明らかになりました。
もともと多少はあるとは思っていましたが、コンパニオン診断が陰性だった患者さんの20~25%ほどが実は偽陰性だったという結果でした。それもあって、特に遺伝子変異を見つけていない患者さんは、偽陰性だとせっかくの分子標的薬が使えないともったいないので、がん遺伝子パネル検査を全例行うようにしています。
藤城
それによって患者さんの予後は延びているという実感はお持ちでしょうか。
鹿毛
かなり実感しています。私が医師になった2000年頃というのは抗がん剤しかないような状況で、そのときは全身状態の良い患者さんであっても平均的な予後は1年というのが通常でした。それが現在、分子標的薬を使うと、薬を飲み続けている期間が1年、2年、3年、一番長いALK阻害薬だと5年という数値も出ていますので、数倍の予後になってきています。
藤城
がん遺伝子パネル検査には幾つか種類があるようですが、その種類と特徴を教えていただけないでしょうか。
鹿毛
現在、固形がんに対するがん遺伝子パネル検査は5種類ありまして、組織を使うものが3つと、血液検査でできるものが2つあります。そのうち組織を使うもの、3つあるうちのひとつが、東京大学で開発したGenMineTOP(ジェンマイントップ)というものです。これは組織を使うものと血液検査と両方セットで行いますので、見つけてきた遺伝子変異ががんに起きているものなのか、それとも生まれつきのものなのかを区別することができます。さらに、この検査では700以上の遺伝子を同時に調べられます。現在、東京大学病院ではこちらをメインに行っています。
また、GenMineTOPはDNAとRNAを両方見る唯一のパネルになっています。特に肺がんにおいては、遺伝子変異だけではなく融合遺伝子を見つけることができたり、発現を見たりすることもできますので、将来性もあるパネルだと思って開発を現在も進めているところです。
藤城
調べられる遺伝子の数が非常に多いということと、DNAとRNAを両方調べられるというところが特徴かと思って拝聴しました。
がんゲノム医療は、今後さらに発展していきそうですが、将来展望について何か教えていただけないでしょうか。
鹿毛
幾つかの方向性があります。一つは、現在のがん遺伝子パネル検査をもっと使いやすく、多くの方に使えるようにするという制度的な面があると思います。やはり診断時に使えないという制約がありますので、それを診断時から使えるようにするとか、現在は三百数十の病院で使えていますが、この数をもっと増やしていくとか、使い勝手を良くしていくことがひとつ大きな面になるかと思います。
もう一つは技術的な面で、ほかにもっとできないかということで、例えば液性検体ですね。細胞診検体や血液検査といった液性検体であると、組織がなくても使え、実際にがん遺伝子パネル検査を受けられる患者さんが増えてきますので、それが大きな進歩になるかと思います。
藤城
確かに肺だと組織を取るのがたいへんだったりしますので、血液検査で調べることができると本当にいいと思いますし、最初の段階からパネル検査が広く使われるようになって、それも全国津々浦々でできるような体制が整うといいですね。
鹿毛先生、ありがとうございました。