大西
肝炎・肝硬変というテーマでお話をうかがいます。
先生は長年、肝臓病学の診療と研究に携わってこられて、肝臓病学の発展や変遷をつぶさに現場で見られていたと思います。かなり変わってきていると思いますが、それを振り返って解説をしていただけますでしょうか。
小俣
もうガラっと変わりました。卒後54年、現在、最前線の病院で患者さんも診ておりますが、昔は、難治性の腹水・静脈瘤の吐血、肝がんの破裂、そして肝性脳症など、消化器内科医の夜はたいへんでした。それが、あまりこの頃は症例がないのです。印象としては5分の1から、もしくは10分の1くらいの印象です。
大西
治療の進歩もかなりあったと思いますがいかがですか。
小俣
半世紀以上前に医師になったのですが、その頃の肝臓病学は代謝性疾患という感じで、間違っても感染症とは思っていなかったと思います。1965年にB型肝炎が(1、2)、1989年にC型肝炎が発見され、日本の7~8割の肝臓病が感染症だと判明しました。それらに対する治療対策が行われた結果、末期的肝臓病が激減した印象があります。
大西
C型肝炎も発見されて、随分治療も変遷してきましたね。
小俣
C型肝炎の発見が1989年、平成元年です(3)。平成の時代が30年続きましたが、C型肝炎は平成に始まり平成に終わったともいえます。すなわち、30年の間にウイルスが発見され、その診断法が確立され、慢性肝炎から肝硬変、そして肝がんへの自然史、すなわち線維化進展とそのスピードを明らかにし(4)、またウイルス駆除により肝線維化が寛解し(5)、肝がんの予防ができることを証明できました。
1992年、千葉大学から東京大学に移り、その間にインターフェロン治療が導入され、一部の患者さんでウイルスの駆除が可能となり、2013年に山梨に異動後、治験を施行し、2015(平成27)年には数週間でほぼ100%ウイルスを駆除できる経口剤の治療薬が完成しました(6、7)。それから10年、先ほども申し上げましたが、非代償性肝硬変、肝がんの劇的な減少につながったと思っています。
大西
これからは脂肪肝といった分野が脚光を浴びるのですね。
小俣
今まではおそらく1~2割がB型、6~7割がC型でした。C型がほぼ消滅すると、残りの1~2割であったアルコールや最近話題のNASHあるいはMASLDと呼ばれているものが割合としては増加し、肝臓病の半分程度はこれら代謝性疾患に起因するようになると考えられます。もちろん、アルコールは依然として重要な原因として残ると考えられます。
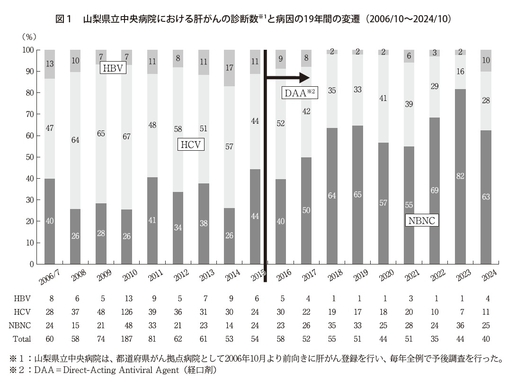
ただ、絶対数が増えるかという問題があります。振り返りますと、2002~2004年が日本の肝がん死亡数のピークで、3万4,000人でした。2023年現在、死亡数は2万2,000人であり、まもなく2万人を切るのではないかと思っています。今後果たしてそれが1万になるのか、あるいは代謝性のMASLD、NASHが増加し、その減少が一定のところでとどまるのか、あるいは逆に増えるのか、予想が難しいと考えています。2009年に私は東京大学を離れ、現在の勤務地である山梨県立中央病院に赴任して16年になります。当院は、都道府県がん、かつゲノム拠点病院であり、そこでの定点観測(図1)からのデータを見ますと、非B非C(NBNC)由来の肝がんのパーセンテージ増加は著しいのですが、図の脚注に示した非B型非C型のがんの絶対数は、必ずしも劇的な増加を示していません(図1)。
現在、生活習慣病に対する治療が進歩していますので、その治療法の進展とのバランスで、究極、日本の肝がん死が1万を切るかどうかとみています。
大西
B型肝炎はどういった治療がスタンダードになっているのでしょうか。
小俣
B型肝炎は1970年代にインターフェロン治療が始まり、1998年に経口剤の核酸アナログが登場しました。ただ、最初の経口剤はYMDD変異耐性株の出現があり(8)、その後、さらに改良が加わり、Entecavirなど、長期にウイルスの増殖を耐性株の出現なく抑制する薬剤が登場し、現在に至っています。ウイルスを抑え込んで肝機能を改善することは現在可能ですが、ただ、残念ながら、ウイルスの完全駆除には至っていません。その一因が、1980年代に我々が明らかにしたcccDNA(Covalently Closed Circular DNA)(9)にあるとされ、40年が経過しました。最近、“Functional Cure”といってHBs抗原の消失を目標とする治療の試みが始まりました。つまり、HBs抗原を消そうというところまで現在来ていると思われます。ただ、それが体内からウイルスの排除、すなわち、組み込まれたDNA(Integrated DNA)の排除となるかは今後の検討課題です。
大西
インターフェロンの位置づけはだいぶ変わりましたか。
小俣
今現在はC型肝炎においてもB型肝炎においても、インターフェロンは使われていません。ただし、インターフェロンをある期間行いますと、その中止後にHBs抗原が消えるという中国からのレポートがあり、先ほどのFunctional Cureを目指すときにインターフェロンを使うということは一部で残っています。このFunctional Cureを目指す薬剤は、新しい機序の、例えばアンチセンスオリゴ(ASO)などを使おうという試みが主流になりそうです。
大西
いわゆるヘルシーキャリアーだと判断する例も多いですが、それを治療すべきかどうか迷うことがあるのですがいかがでしょうか。
小俣
そのとおりです。日本では現在、患者さんが重症な劇症肝炎(10)を発症する、あるいは、進行性のB型慢性肝炎病変を有しているという事例は少なく、積極的な治療の動きはありません。一方、中国はいかんせん数が多いので、B型肝炎研究はワクチンと同様に国家的な事業として新たな薬剤の研究開発が盛んに行われているという状況です。
大西
かつてはC型肝炎にインターフェロンでの治療が相当行われたと思いますが、今の治療のスタンダードはどのように考えたらよいでしょうか。
小俣
これも1982年にcDNAの断片がクローニングされ、先に述べた治療法(経口剤)の開発につながりました(6、7)。インターフェロンは長らく多様な治療法で試みられましたが、そのウイルス駆除率は10~15%程度でした。しかし、2013年より新たな経口剤による治験が行われ、駆除率も95%から100%へと上昇し(6、7)、2015年に経口剤(8~12週間の投与)で全例でのウイルス駆除を目指した保険診療が開始されました。それから10年が経って今の私の外来はウイルスが消えたSVR(Sustained Virological Response)の患者さんがほとんどです。線維化寛解の様子(5)をFibroScanという機器で診ながら、肝がん発生の有無を調べる外来に変わりました。私が卒業した50年前には、肝臓外来には70歳を超す方はそれほどいませんでしたが、現在は肝硬変で色が黒くなり、お腹に水が溜まった非代償性肝硬変という方は、ほとんどいません。C型肝炎の話をすると「私はかつてインターフェロンで頑張ったけれどもだめで、その後、経口剤のおかけで助かりました、ありがとうございます」という感じの外来です。
大西
もうインターフェロンは役割を終えたのでしょうか。
小俣
先ほどのB型肝炎での短期的治療によるHBs抗原消失を目指す中国の試み以外はあまりないと思われます。C型肝炎ではありません。
大西
経口剤でC型肝炎ウイルスを駆除したケースでも、その後に何か問題となる場合はありますか。
小俣
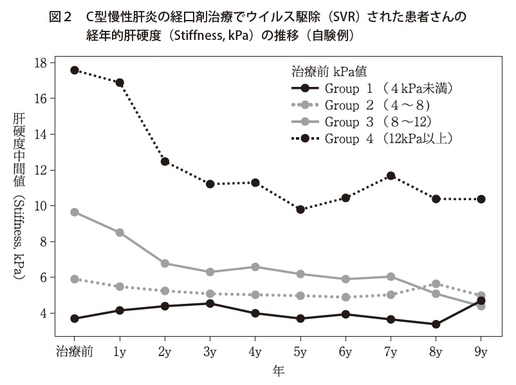
たいへん重要な質問です。また、目下の課題です。高齢化と相まってウイルスが消えたら肝がんにならないという単純な図式ではありません。頻度は落ちていますが、実は肝がんは発生します(11)。重要な点は、現在、肝生検の代わりに前述のFibroScanという機械がありますので、肝の硬さ(Stiffness)、あるいは線維化(Fibrosis)を簡単に非侵襲的に測ることができます。つまり、かつては肝生検でしたが、そのFibroScanの機械で具体的な数字によって線維化進展の、あるいは退縮(Regression)(5)で線維化のStageの評価ができます。12kPa(パスカル)以上は肝硬変と考えられますが、この集団のStiffness(硬さ)はなかなかウイルスが消えても戻らないというのが、我々のデータです(図2)。一方、12kPa以下の人は、正常域は4~6なのですが、正常域まで戻る頻度は高いといえます。したがって肝がんの発生については、ベースラインの肝臓の硬さが12kPa以上の方は丁寧にフォローしないといけない。すなわち、時が経っても10kPA以上で推移し(図2)、発がんリスクは依然として高いといえます。
気持ちとしては「あなたは完全に治りましたよ」と言いたいのですが、肝臓の傷(線維化)は残っているので「要注意ですよ」と患者さんに伝えています。
大西
ご年配の肝臓がんの方もいらっしゃいますよね。
小俣
ですから、硬さと年齢、その2つのファクターで注意されたほうがよいと思います。
大西
肝硬変では何か新しい治療の進歩はありますか。
小俣
今まで申しましたように、ウイルス駆除によっての予防という点で、非代償性肝硬変へ進展する患者さんは激減しました。一方、世界に目を向けると、アジアは全世界の肝硬変、肝がん発生数の3分の2を占めており、ガイドライン作成(12)を含め多様な対策をとっています。中でも肝硬変、肝がんの治療に関しては、中国を中心として肝移植が極めて日常的な医療となっている点が、特記すべき事柄だと思います。
大西
ウイルスの治療も肝硬変で積極的にやられるようになっているのでしょうか。
小俣
今回まとめましたが、がんになった方のC型肝炎ウイルスを駆除すると、もちろんがんの治癒・切除等行われたということが条件ですが、劇的に生命予後がよくなります。生命予後が改善するというのは、がんの発生を抑える点と、肝不全への予防効果という肝全体へのトータルの影響ではないかと考えます。
大西
先生のお話をうかがうと、だいぶ変わってきたことを実感します。これから外来で肝臓を診る医師に向けて、何かメッセージはありますか。
小俣
我々は、C型肝炎などのウイルス感染から、がん発生への道のりのいわば“自然経過”を明らかにし(4)、高危険群の設定を行い、さらには抗ウイルス療法による線維化の寛解(5)、ひいてはがんの発生の予防という研究を長年やってきました。今後は、MASLDあるいはNASHの領域でC型慢性肝炎と同様ながんへのNatural Courseを明らかにし、その予防対策の効果を検証することが肝臓病学の最大の眼目と考えられます。すなわち、極めて多数おられるMASLDの患者さんにとってどの型が本当に危ないのか、肝がんリスクが高いのかを解明することが大命題です。
大西
難しいですよね。
小俣
難しいです。ですから、そこをいろいろなモダリティー、研究手法を用いて明らかにする。今後の極めて困難で、かつ重要なテーマだと考えています。
大西
かえって困難な感じがしますけれども。
小俣
そのとおりですね。頻度の低い中からピンポイントでどの方ががんになるかと同定するのは、大袈裟にいいますと、自然科学の中でも最も難しい領域ではないかと考えられます。これはもしかしたら、ウイルスという小さな遺伝子から、さらに大きなゲノム解析( Human Genome)に挑戦せよ(13)というHepatologistsへのメッセージかもしれません。また、医療経済的にも極めて重要なテーマと考えています。
大西
画像検査をまめにチェックしなければいけないなということは感じます。
小俣
肝がんの早期発見の方法としては、日本には素晴らしい腫瘍マーカーが3つ(AFP、AFP-L3、PIVKAⅡ)あります。これは、世界に誇れる、しかも保険でカバーされているという点で、日本の肝がん診療の特色は、その早期発見の能力に優れている点と考えられます。これは、がんの多いアジアの国々にも広く喧伝されています(12)。今まで述べたNASH、MASLDの発がんは、それら高危険群の決定のために、さらなる基礎研究、および臨床応用が強く望まれる領域である点を再度申し述べたいと思います。
大西
小俣先生、本日はたいへん興味深いお話をありがとうございました。
文献
(1)Omata M, Peters RL, et al. Hepatocellular carcinoma in the USA, etiologic considerations. Gastroenterology. 1979; 76: 279-287.
(2)Omata M, Peters RL, et al. Comparison of serum HBsAg and serum anticore with tissue HBsAg and HBcAg. Gastroenterology. 1978; 75: 1003-9
(3)Omata M, Ito Y, et al. Interferon therapy in acute non-A, non-B hepatitis. Lancet. 1991; 338: 914-915.
(4)Yoshida H, Omata M, et al. Interferon therapy reduces the risk of hepatocellular carcinoma; national surveillance. Ann Int Med. 1999; 131: 174-181.
(5)Shiratori Y, Omata M, et al. Histologic improvement of fibrosis in patients with hepatitis C by interferon. Ann Int Med. 2000; 132: 517-524.
(6)Mizokami M, Omata M, et al. Direct-acting antivirals for hepatitis C virus infection in Japan. Lancet Infect Dis. 2015; 15: 645-653.
(7)Omata M, Mizokami M, et al. Sofosbuvir plus ribavirin in Japanese patients with chronic genotype 2 HCV infection: an open-label, phase 3 trial. J Viral Hepat 2014; 21: 762-768.
(8)Omata M. Treatment of chronic hepatitis B infection (Editorial). N Engl J Med 1998; 339: 114-115.
(9)Yokosuka O, Omata M, et al. Covalently closed circular DNA of hepatitis B virus. Hepatology. 1985; 5: 728-734.
(10)Omata M, et al. Pre-core mutant hepatitis virus and fulminant hepatitis. N Engl J Med. 1991; 324: 1699-1704.
(11)Obi S, Omata M, et al. The incidence of all organ malignancies and overall survival of patient with sustained virological response of HCV-comparable to SMR (standardized mortality ratio) of Japan general population. Hepatol Int. 2023; 17: 562-572.
(12)Omata M et al. Asia-Pacific clinical practice guidelines on the management of hepatocellular carcinoma: a 2017 update. Hepatol Int. 2017; 11: 317-370.
(13)Tateishi R, Omata M. Hepatocellular carcinoma in 2011: Genomics in hepatocellular carcinoma -a big step forward. Nat Rev Gastroenterol Hepatol. 2012; 9: 69-70.